개인적으로 입사후에도 정말 헷갈렸던 부분인 것 같아요 ㅠㅠ
SDV라는 개념과 QC랑 관련된 파트가 정말 일상에서
겪어볼 일이 없다보니 어려웠네요 ㅎㅎ...

<GCP점검 및 실태조사>
임상시험 GCP 점검
- 임상시험의 설계 -> 수행 -> 기록 -> 보고에 대한 윤리적/과학적 기준을 제시하는 것이 의약품 임상시험 관리기준(KGCP)
- GCP 가이드라인에는 의뢰자, 시험자에 대한 업무에 대해 적혀 있음
- 품질보증과 품질관리
# 의뢰자: 임상시험의 수행, 자료의 생산, 기록, 보고 등 계획서, GCP, 관계 규정에 따라 진행
# 품질관리: 품질보증체계의 한 부분으로서 임상시험과 관련된 행위나 활동이 적절한 수준(임상시험 계획서 등에서 정한 대로)에서 이뤄지고 있음을 검증하는 행위나 기법 -> 행위 한 후에 확인하는 사후관리 개념~
# 품질보증: 임상시험, 자료의 수집, 기록 및 문서 작성, 보고 등에 관한 사항이 GCP와 관계법령을 준수하였는지 여부를 사전에 계획된 바에 따라 체계적으로 확인하는 활동, 품질관리보다 큰 개념
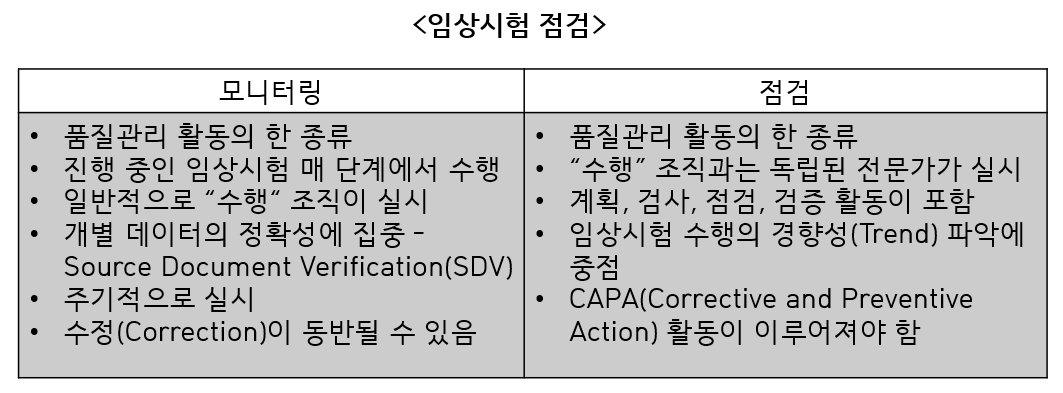
- 임상시험 점검
# 임상시험이 임상시험계획서, 의뢰자의 표준작업지침서(SOP), 관계 규정을 준수하여 수행되는지 조사 + 자료가 정확히 기록, 분석, 보고되는지 조사
# KGCP에서는 정규적인 모니터링 혹은 품질관리 활동과는 독립적으로 구분해서 audit을 수행하도록 결정함
# 점검자(Auditor): 의뢰자가 지정하는 임상시험 수행과 독립된 전문가여야 하고, 점검자는 해당 임상시험과 이해관계가 없어야 함
# 의뢰자는 GCP 가이드라인 점검지침을 통해 점검을 수행하고 점검결과보고서를 작성
# 임상시험 점검 결과 미흡한 부분이 있다면 CAPA 활동을 통해 개선하게 됨
⊙ CAPA(시정활동+예방활동): 표준작업지침서나 규정에 부합하지 않는 업무 개선 활동
⊙ 시정활동: 확인된 문제 원인을 제거해서 문제가 재발하지 않도록 함(잘못된 자료가 수집된 경우 잘못 잘못된 자료가 더 수집되지 않도록 절차개선) Cf. 수정활동: 잘못된 자료가 수집된 경우 잘못 수집된 자료를 바로잡는 것
# 임상시험 점검이 끝나면 점검자는 점검확인서를 작성하여 의뢰자에게 전달함
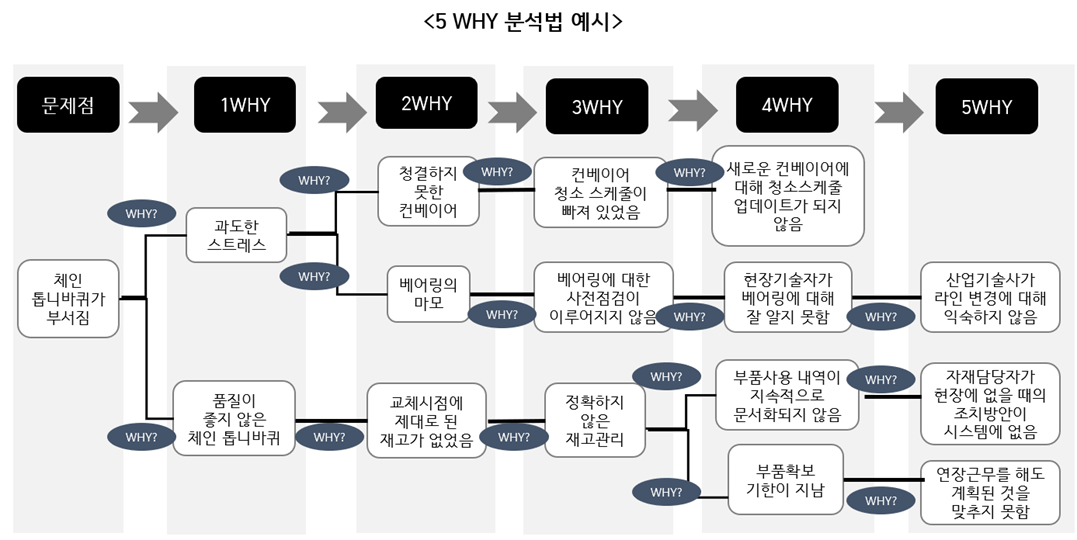
- 근본원인 찾는 방법(5why 분석법)
# 왜 그 문제가 발생했는지 근본원인 찾을 때까지 계속 질문
# 보통 다섯번 정도 질문하면 근본원인에 도달
# 한가지 현상에도 여러 개의 원인 존재
# 문제에 따라 질문의 수가 5번보다 적을 경우도 존재함
임상시험 실태조사와 후속조치
- 실태조사: 임상시험을 수행하는 사람이 준수사항을 잘 지키면서 임상시험을 수행하였는지를 식품의약품안전처장이 확인하는 절차(임상시험 실시기관, 의뢰자, 또는 수탁기관 등의 모든 시설, 문서, 기록 등을 확인하는 것)
- 임상시험 실태조사의 종류
① 정기점검: 주로 임상시험실시기관의 운영실태에 대해 정기점검, 임상시험 의뢰자에 대해서도 점검함
② 품목점검: 임상시험 결과를 근거로 품목허가 신청이 있을 때 해당 임상시험에 대한 조사를 실시
③ 특별점검: 특정 사안에 대해 조사할 필요가 있을 때(사회적 이슈, 민원 있을 때)
- 후속조치의 종류
# 위반 -> 행정처분이 진행됨
⊙ 규정을 위반한 정도가 시험대상자의 안전/권리/복지나 임상시험 결과의 품질, 완결성에 부정적 영향을 미친 경우
⊙ 임상시험 자료의 심각한 품질저하나 중요 근거문서의 부재, 자료의 조작 또는 의도적인 왜곡 등 확인된 경우
# 시정
⊙ 일부 임상시험과 관련된 미흡한 부분이 있었지만 결과적으로 시험대상자의 안전/권리/복지나 임상시험 결과의 품질, 완결성에 부정적 영향을 미치지는 않았으나 가능성이 큰 경우
⊙ 임상시험 자료의 경미한 품질저하, 비중요 근거문서의 부재, 반복적으로 발생한 경미한 규정 미준수 사항 등이 확인된 경우
# 주의
⊙ 임상시험과 관련된 미흡한 부분이 시험대상자의 안전/권리/복지나 임상시험 결과의 품질, 완결성에 부정적인 영향을 미칠 가능성이 있는 경우
# 권고
⊙ 규정의 미준수 사항은 아니지만 향후 임상시험의 품질을 높이고 미준수 가능성을 줄이기 위한 제안
파잇팅..!
'다람이는 공부중 > #0 임상시험의 기본' 카테고리의 다른 글
| 임상시험 Konet 강의 -11(임상시험/근거문서 및 CRF의 이해) (2) | 2022.09.23 |
|---|---|
| 임상시험 Konet 강의 -10(임상시험/임상시험 준비-그외) (0) | 2022.09.22 |
| 임상시험 Konet 강의 -9(임상시험/임상시험 준비-계획서의 이해) (0) | 2022.09.21 |
| 임상시험 Konet 강의 -8(임상시험/심사위원회 업무의 이해) (0) | 2022.09.21 |
| 임상시험 Konet 강의 -6(임상시험/이상반응보고 및 관리) (0) | 2022.09.19 |
| 임상시험 Konet 강의 -5(임상시험/의약품 개발) (1) | 2022.09.18 |
| 임상시험 Konet 강의 -4(임상시험/안전성 관리) (0) | 2022.09.17 |
| 임상시험 Konet 강의 -3(임상시험/대상자 동의 및 대상자별 고려사항) (0) | 2022.09.17 |
