다음은 면접에서 가장 많은(?) 질문을 받게되는
SAE 그리고 SUSAR 관련 내용입니다람쥐

<안전성 관리>
용어
https://lovingmylife.tistory.com/10?category=954998
clinical study(임상시험) -5
드디어 마지막! 여기까지 오시느라 고생 많으셨어요(_ _) 마지막까지 힘내볼까요! 8. AE란? - AE adverse event 이상반응 -> 약물과 관련 없이도(IP와 인과관계 필요 x)이상 반응이 있는 것을 말해요. - AD
lovingmylife.tistory.com
시험책임자 및 시험의뢰자의 의무와 책임
- 시험책임자의 의무
- 임상시험책임자: 임상시험 중 발생하는 모든 AE에 대해 임상시험계획서 및 KGCP에 따라 철저히 수집, 평가 및 보고, 수행해야함
# 시험책임자는 즉시 보고하지 않아도 된다고 따로 정한 것을 제외한 모든 중대한 이상반응에 대해 신속히 의뢰자에게 보고해야함, 보통 24시간 내에 fax나 전자문서 등으로 보고
# 대상자 신상에 관한 비밀 보호를 위해 시험대상자 식별코드를 사용해야 함
- 의뢰자
# 이상반응 보고 받은 경우: 이상반응 보고와 관련된 자세한 내용을 임상시험계획서에 반영, 필요한 경우 별도의 지침 제공, KGCP와 IRB 규정 등에 따라 IRB에도 보고
# 임상시험용 의약품의 안전성에 대한 평가를 지속적으로 실시
# 시험대상자의 안전과 권익 보호를 위해 안전성 정보를 지속적으로 모니터링, 평가, 관리
# 새로운 중요한 안정성 정보 취득 시 신속히 규제기관(식약처장)에게 보고
- 임상시험 업무수행자(CRC 포함): 시험책임자가 설명한 업무 준수 -> 위임 받은 업무 철저히 수행할 것
임상시험 안전성 정보의 보고

- 시험자는 의약품과의 인과관계나 예측가능성 등과 관계없이 중대한 이상반응이 나타나게 되면 모두 보고!! -> 임상시험 계획서와 IRB SOP에서 정하는 기한 내에 각각 의뢰자와 IRB에 보고
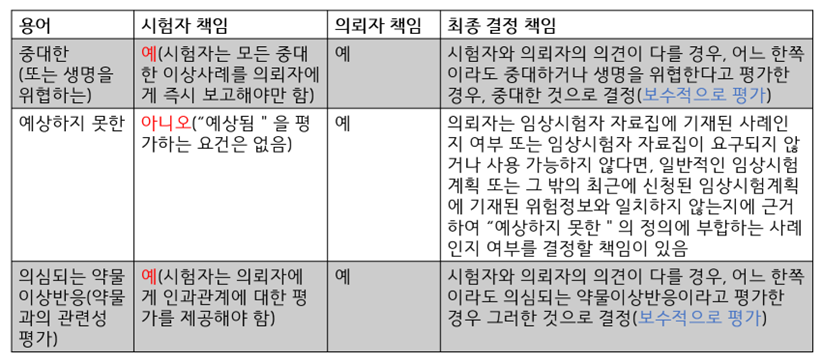
- SUSAR 보고기한
# 사망 초래하거나 생명 위협하는 경우 : 의뢰자가 해당 사실을 보고 받거나 알게된 날부터 7일이내, 단 의뢰자는 정보가 모두 보고되지 않은 경우 추가 정보는 최초로 해당 사실 보고받거나 알게된 날부터 15일 이내
# 그 밖에 중대한 예상하지 못한 약물 이상반응의 경우 의뢰자가 해당 사실 보고 받거나 알게된 날부터 15일 이내
- SUSAR 보고 시 중대성, 약물과의 관련성, 예측성의 기준, 범주, 평가방법음 “임상시험계획서, 임상시험자 자료집”이 기준이 됨
- 추적보고
# 초기보고한 약물 이상반응에 추가정보가 존재하면 종결시까지 보고해야함(종결: 해당 약물이상반응이 사라지거나 추적조사가 불가능하게 되는 것)
# 임상시험 진행 중 발생한 SUSAR의 초기보고 기준: 식약처장으로부터 임상시험계획 승인을 받은 날부터 식약처장에게 임상시험 종료 보고시까지 보고하는 것이 원칙
# 이미 보고한 SUSAR 사례 추적보고: 임상시험 종료 보고를 하였더라도 해당 사례가 종결될 때까지 가능한 한 계속 보고
- 임상시험자 자료집
# 내용: 원료의약품 및 제형, 동물에서 약물의 약리, 약동, 독성, 생물학적 특징 및 효과, 이전 임상시험을 통해 얻은 사람에서의 안전성 및 유효성과 관련된 정보 등
# 예측가능성을 평가하는 기준으로 사용됨
'다람이는 공부중 > #0 임상시험의 기본' 카테고리의 다른 글
| 임상시험 Konet 강의 -8(임상시험/심사위원회 업무의 이해) (0) | 2022.09.21 |
|---|---|
| 임상시험 Konet 강의 -7(임상시험/GCP점검 및 실태조사) (1) | 2022.09.19 |
| 임상시험 Konet 강의 -6(임상시험/이상반응보고 및 관리) (0) | 2022.09.19 |
| 임상시험 Konet 강의 -5(임상시험/의약품 개발) (1) | 2022.09.18 |
| 임상시험 Konet 강의 -3(임상시험/대상자 동의 및 대상자별 고려사항) (0) | 2022.09.17 |
| 임상시험 Konet 강의 -2(임상시험/KGCP) (1) | 2022.09.16 |
| 임상시험 Konet 강의 -1(임상시험/규정의 이해) (4) | 2022.09.15 |
| 임상시험 관련 포스팅 예정 목록 (0) | 2022.09.15 |
